Sclérose en plaques : qu’est-ce que c’est ?
La sclérose en plaques est marquée par la destruction ou la raréfaction de la gaine protectrice des neurones, c’est-à-dire la myéline, qui est remplacée par de la fibrose ou de la sclérose disséminée de façon totalement anarchique.
La sclérose en plaques est l’affection neurologique dégénérative centrale la plus fréquente et pour le public peut-être, la plus mal vécue, celle dont l’appréciation reste des plus péjoratives. Elle touche une population jeune et les termes de « sclérose en plaques » sont associés à l’image d’un handicap pouvant aller jusqu’à la perte de l’autonomie personnelle.
Cette opinion mérite d’être, sinon combattue, du moins nuancée, car cette extrapolation péjorative vis-à-vis de la maladie résulte de la projection vers les formes graves et invalidantes qui ne représentent qu’un quart environ de l’ensemble des malades atteints. Inversement, les formes totalement bénignes, non handicapantes, et dont le pronostic est favorable pour le restant de l’existence, sont méconnues.
En France, 40 à 50 000 personnes en souffrent
Sur le plan statistique, entre 40 000 et 50 000 Français souffrent de cette affection et chaque année, environ deux nouveaux cas sont diagnostiqués pour 100 000 habitants. L’âge d’apparition de l’affection se situe entre 20 et 45 ans, tout en sachant que des formes infantiles ou tardives (chez les personnes ayant atteint la cinquantaine), sont possibles mais rares.
La répartition géographique de l’affection est inégale et la maladie est plus présente au nord qu’au sud de la France.
On peut aujourd’hui agir sur la maladie
L’approche thérapeutique de la sclérose en plaques repose sur un travail actif et coopératif essentiel entre le médecin traitant, le neurologue et le malade, en sachant qu’aujourd’hui nous ne sommes plus contemplatifs et les bras baissés. Nous disposons d’armes thérapeutiques nouvelles et efficaces bien que l’étiopathogénie (autrement dit la recherche de l’origine et de l’évolution de la maladie) et l’agent infectieux initial ne soient pas clairement identifiés.
Ce travail de collaboration suppose un diagnostic qui doit être établi de façon certaine et évidente, aidé par les deux examens indispensables que sont l’imagerie par résonance magnétique (IRM) et l’exploration par ponction lombaire du liquide céphalo-rachidien (LCR), la connaissance des nouveaux traitements et de ceux à venir.
Un traitement de fond existe depuis 1996 en France
Le pessimisme qui entoure cette maladie doit être encore plus nuancé depuis 1996. A cette date a été introduit et prescrit en France un traitement de fond, l’interféron bêta qui éloigne ou écarte les poussées de la maladie pour en fin de compte réduire de façon notable le handicap fonctionnel.
Cette approche thérapeutique nouvelle qui doit s’appliquer très tôt dans l’apparition de la maladie – ce que nous appelons la deuxième poussée – impose un diagnostic précis de l’affection et une information lucide et éclairée du patient qui est largement impliqué dans le programme thérapeutique. C’est dire toute l’importance du dialogue constant entre le médecin et le malade !
Sclérose en plaques : comment la reconnaître ?
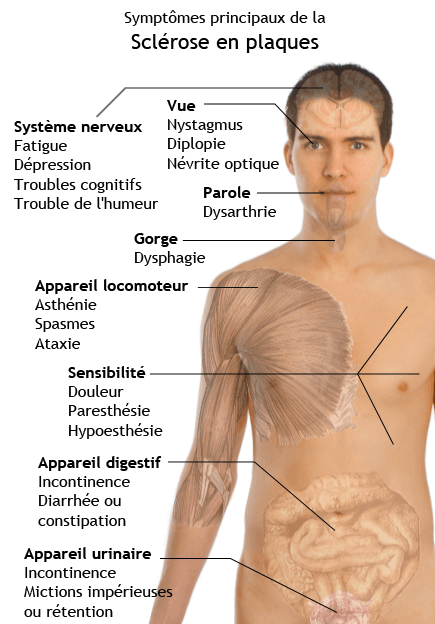
Il s’agit d’une affection déroutante. Elle s’exprime sous différentes formes, aussi bien dans le temps que dans ses symptômes, rendant la comparaison ou l’extrapolation d’un malade à un autre impossible.
On peut dire que toute atteinte neurologique régressive (qui disparaît d’elle-même) peut correspondre au départ à un mode de début d’une sclérose en plaques, ce qui peut inquiéter la plupart des gens. Toute manifestation neurologique survenant entre 15 et 50 ans environ (mais des formes infantiles ou plus tardives sont possibles) peut être l’expression primaire de la maladie. Cette dernière, dans l’immense majorité des cas, se résout spontanément en quelques semaines, même sans traitement ! Cette maladie débutante peut donc être par la suite ignorée et ne pas induire un bilan neurologique plus précis.
Des indices existent
Il est cependant des cas où il est possible d’évoquer la sclérose en plaques : baisse brutale de la vision liée à la névrite optique rétro-bulbaire (atteinte du nerf optique) et qui pourrait faire penser à tort à une maladie ophtalmologique, troubles de la coordination ou de l’équilibre, sensations de picotements diffus constants des quatre membres (paresthésies), douleurs de la moitié du visage surtout accompagnées d’une diminution de la sensibilité de la face.
Par la suite, après quelques années de latence, l’affection évolue par des étapes fécondes de la maladie appelées « poussées ». Elles peuvent être très distantes les unes des autres dans le temps, de plusieurs années parfois, et la maladie ne se manifeste pas pendant ce laps de temps. Après sept ans environ de ce silence, elles peuvent se succéder, et c’est alors de toute évidence le moment propice pour introduire le traitement préventif au long cours en utilisant une des trois formes disponibles de l’interféron bêta.
L’approche de la maladie s’est modifiée ces dernières années. Les médecins hésitaient à établir le diagnostic dès le départ, alors même que l’évolution est généralement favorable, pour éviter d’entretenir l’angoisse chez le malade. Aujourd’hui, il est possible de réaliser les examens complémentaires plus précocement puisque le diagnostic débouche forcément sur une attitude thérapeutique.
La période « d’état »
Après plusieurs années sans poussées ou marquées de poussées résolutives laissant peu de grandes séquelles pour le malade, l’affection entre en général dans sa période d’état. L’évolution se fait alors fort variable. On distingue :
- les formes « rémittentes » qui évoluent par poussées, laissant plus ou moins de séquelles ;
- les formes progressives continues où le handicap évolue péjorativement sans poussée nettement individualisable ;
- les formes secondairement progressives dans lesquelles, après quelques poussées et en général après sept à huit ans d’évolution de la maladie, on observe une progression soit d’un seul tenant sans poussée, soit au contraire avec des poussées, mais laissant chacune des séquelles qui aggravent et se greffent à celles préexistantes.
Il faut savoir que les formes rémittentes représentent plus de trois quarts des formes d’évolution dans la phase d’état de la maladie. C’est à elles que s’adressent d’une part les traitements de la poussée (les fameuses perfusions intraveineuses de corticoïdes à fortes doses appelées aussi bolus), d’autre part les médicaments qui stoppent ou enrayent les poussées et les séquelles handicapantes qui en sont la conséquence (les interférons).
Une intrication de signes pathologiques
Dans cette période dite d’état existe une intrication de signes pathologiques.
Des troubles de la coordination donc une maladresse du geste manuel, de l’équilibre, avec en particulier une démarche ébrieuse (semblable à celle d’un ivrogne) surtout lorsque le contrôle visuel est supprimé.
Des troubles de la marche avec une faiblesse et des difficultés manifestes à se déplacer rendant la personne parfois dépendante.
Des troubles sphinctériens avec soit impossibilité de retenir les urines soit au contraire une envie impérieuse d’uriner.
Des troubles dans la reconnaissance de la position des extrémités des membres par rapport au reste du corps (segments distaux du schéma corporel). Selon le tableau exact et les différents signes présentés par le malade, on parlera alors de syndrome cérébelleux, vestibulaire central, pyramidal ou cordonal postérieur.
Des symptômes aux formes multiples
La multiplicité des symptômes et leur diversité rendent impossible la comparaison d’un malade par rapport à l’autre, tant sur le plan de son expression clinique que sur sa gravité et son évolutivité future. C’est un point très particulier de cette maladie.
Rappelons par exemple qu’un quart ou un cinquième des malades souffrant de sclérose en plaques dûment certifiée sont des scléroses en plaques bénignes. Connaissant une seule poussée, régressive, et n’entraînant pas de réel handicap dans la vie sociale ou professionnelle, celles-ci peuvent faire que le patient oublie jusqu’à l’épisode initial après dix à vingt ans d’évolution sans aucun traitement de fond !
Sclérose en plaques: quels examens ?
Deux examens sont indispensables, l’imagerie par résonance magnétique (IRM) et l’exploration par ponction lombaire du liquide céphalo-rachidien. D’autres permettront de confirmer le diagnostic : les « potentiels évoqués ».
Un certain nombre d’examens vont permettre d’affirmer avec la plus forte probabilité le diagnostic de sclérose en plaques : potentiels évoqués visuels, auditifs, et plus largement toutes les perceptions sensorielles ressenties consciemment au niveau musculaire et articulaire, ou au niveau de la peau et des viscères (somesthésiques). Deux examens sont indispensables, tout en sachant que ni l’un ni l’autre ne sont totalement spécifiques, même s’ils sont compatibles, car il convient aussi de procéder dans le même temps à l’exclusion des autres maladies dites démyélinisantes.
Deux examens indispensables
L’imagerie par résonance magnétique (IRM) révèle des hyposignaux en T1 (temps de relaxation longitudinal) et des plages d’hypersignal périventriculaires en T2 (temps de relaxation transversal). Il est utile de compléter cet examen encéphalique par une étude si possible de la moelle selon les points d’appel. La présence de ces hypersignaux en T2 sur l’IRM encéphalique n’est pas totalement spécifique de la sclérose multiloculaire. Il sera demandé en général l’injection d’un produit de contraste, non allergisant (Gadolinium) pour disposer de renseignements plus complets. L’IRM est un examen facilement réalisable et généralement pratiqué en ambulatoire.
L’exploration par ponction lombaire du liquide céphalo-rachidien est aussi indispensable. Elle nécessite une ou deux journées d’hospitalisation et peut objectiver des signes spécifiques à la sclérose en plaques (une réaction cellulaire mononuclée et surtout une synthèse intrathécale des immunoglobulines au sein même du liquide céphalo-rachidien).
Dans le même temps, cette exploration permettra d’éliminer les affections qui ressemblent à la sclérose en plaques mais qui sont totalement différentes (ce que ne permet pas l’IRM), en particulier les complications neurologiques centrales de certaines maladies infectieuses ou inflammatoires.
Sclérose en plaques: comment cela marche-t-il ?
La sclérose en plaques est marquée par la destruction ou la raréfaction de la gaine protectrice des neurones, c’est-à-dire la myéline, par un processus inflammatoire délétère et régi par des mécanismes auto-immuns. Cette myéline détruite est remplacée par de la fibrose ou de la sclérose disséminée de façon totalement anarchique expliquant la variété des formes sous laquelle la maladie peut se présenter (polymorphisme) tant dans le temps que dans l’espace.
Sur le plan neurochimique, la maladie est caractérisée par une cascade d’événements immunologiques aboutissant à la destruction disséminée et polymorphique de cette gaine de myéline, d’où le nom de maladie démyélinisante (dans laquelle la myéline est remplacée par de la sclérose cicatricielle).
Il existe un antigène
Il existe donc bien un antigène, éventuellement bactérien ou viral, et chacun d’entre nous peut être (et est vraisemblablement) à son contact. Mais chez les patients atteints de sclérose en plaque, cet antigène qui normalement n’est pas reconnu et est donc inoffensif, est happé par le système immunitaire présent au niveau du système nerveux central et représenté par les macrophages et les lymphocytes. Il passe donc la barrière hémato-encéphalique normalement impénétrable, aidé par ce que nous appelons les molécules d’adhésion. Et de ce combat entre l’antigène et le système immunitaire au niveau de la substance blanche, sont générées des substances pro-inflammatoires toxiques détruisant la myéline, puis, dans un second temps, le fil conducteur de l’influx nerveux : l’axone.
La gravité de l’évolution de la maladie dépend d’ailleurs de l’étendue de l’atteinte axonale. S’il existe donc bien un antigène supposé auquel nous sommes tous exposés, ni le franchissement ou 1’altération de la barrière hémato-encéphalique, ni la cascade immunologique qui s’ensuit n’existent chez un individu non atteint.
Débusquer l’antigène
Cela complique singulièrement l’avancée dans la recherche. C’est pourquoi on reproduit l’affection chez l’animal, par injection de substances allergisantes. On peut induire des signes similaires à ceux d’une encéphalopathie expérimentale allergique superposable à la sclérose en plaques humaine. Mais les recherches n’ont pas abouti à la reconnaissance d’un antigène-candidat mis en cause de façon certaine. L’espoir demeure avec, s’il est « débusqué », la possibilité d’une éventuelle action thérapeutique ou d’un vaccin.
L’interféron bêta qui est proposé agit aussi bien au niveau de la barrière hémato-encéphalique qu’en abaissant la production des substances délétères témoins de l’inflammation et myélinotoxiques. Par contre, le traitement proposé lors des poussées, les perfusions de corticoïdes à fortes doses, est destiné essentiellement à maintenir l’intégrité de la barrière héméto-encéphalique pendant de nombreuses semaines.
Sclérose en plaques: quels risques ?
La maladie dépend de facteurs dits environnementaux, sans que nous sachions très exactement lesquels sont impliqués dans le déclenchement de la maladie. En France, au nord du 45° parallèle environ, l’affection est deux à trois fois plus fréquente à population égale que dans le Sud. Il serait tentant bien entendu d’y voir une influence climatique mais il n’en est rien.
Dans les zones où l’on compte un nombre faible de cas rapporté à la population totale (la prévalence), existent des régions et des villes fortement atteintes (Avignon en France, la Sardaigne dans le bassin méditerranéen). La même remarque s’applique dans l’hémisphère sud où l’atteinte est fréquente dans les zones tempérées (Australie et Nouvelle-Zélande), inexistante dans celles chaudes et tropicales.
L’influence des flux migratoires
L’étude des mouvements migratoires des populations montre que l’affection prédomine chez des populations comportant un nombre important de personnes venues des zones géographiques fortement exposées. Ces mouvements migratoires expliquent les « nids » de forte prévalence au milieu d’une population peu exposée. La forte surreprésentation de la maladie aux USA dans certains Etats comme le Minnesota par exemple, qui se trouve à une latitude identique à celle du sud de la France, est partiellement expliquée par le fait que la population est composée de nombreux descendants d’émigrés des pays nordiques. Ces déplacements migratoires liés à l’historicité expliquent certains foyers de la maladie au Moyen-Orient, en particulier au Koweït, mais là ce sont les descendants des croisés qui sont exposés !
Ces facteurs environnementaux ne sont pas suffisants pour expliquer à eux seuls la maladie et il serait illusoire de penser qu’un malade atteint de sclérose en plaques pourrait se trouver amélioré en déménageant vers le sud ou qu’inversement le fait d’être déplacé vers les régions nordiques pour un Méditerranéen pourrait le conduire à être davantage exposé.
Le lieu de résidence des quinze premières années de la vie joue un rôle important
La seule certitude scientifique est la probabilité et la prévalence des personnes selon qu’elles ont vécu dans les quinze premières années de leur vie dans les régions exposées, donc au nord du pays par rapport au sud, peu ou moyennement exposées.
Nous savons simplement que si nous avons vécu dans ces quinze premières années de la vie au nord nous avons trois fois plus de malchances de contacter la maladie même si par la suite nous sommes à même d’être déplacés vers le sud.
La même probabilité inverse s’applique aux personnes ayant vécu les 15 premières années de leur vie en dessous du 45e parallèle où elles ont trois fois plus de chances de ne pas contacter la maladie ! Ces statistiques ont été totalement confirmées aux États-Unis où les mouvements migratoires liés aux déplacements professionnels sont particulièrement nombreux. Les facteurs environnementaux sont donc importants, mais non décisifs.
Les facteurs environnementaux
L’habitation, l’alimentation, le mode de vie ou un éventuel toxique (industriel) ne semblent pas en cause. Il s’agit donc plus d’un agent infectieux probable (viral ? bactérien ? toxique ?) qui induit, sur un terrain génétiquement prédisposé, la série des cascades pathologiques aboutissant à l’atteinte démyélinisante du système nerveux central qui est celle de la sclérose en plaques. De nombreux candidats infectieux ont été, et seront encore, proposés comme étant le primum movens de l’affection.
Il conviendra d’être d’une grande prudence avant que de leur reconnaître de façon décisive à l’avenir un rôle pathogène inducteur ! L’exemple éloquent très récent est celui des supposées scléroses en plaques apparues après une vaccination contre l’hépatite B chez des enfants ou adolescents dont l’un des parents souffrait de la maladie. Aujourd’hui, il n’existe aucun argument scientifique prouvé démontrant que la vaccination contre l’hépatite B peut induire une sclérose en plaques.
Cependant, toute stimulation immunitaire comporte le risque d’induire une poussée chez les patients atteints de sclérose en plaques. Ainsi, par mesure de précaution, le ministère de la Santé a décidé de considérer que, pour les personnes atteintes de sclérose en plaques ou ayant des antécédents familiaux de SEP (risque de SEP plus élevé), le bénéfice de cette vaccination doit être évalué au cas par cas par le médecin traitant, en fonction des risques d’exposition au virus et du risque encouru de SEP.
Les facteurs génétiques ne doivent pas être négligés
Les facteurs génétiques stricto sensu sont de la même espèce, à savoir non négligeables, mais ne permettant pas d’expliquer la maladie. L’illustration en est apportée par l’étude des jumeaux ou jumelles homozygotes donc identiques sur le plan génétique, des « clones » : si l’un développe la sclérose en plaques, l’autre ne la développera qu’une fois sur quatre, ce qui ne correspond à aucun critère génétique. Cela exclut l’hypothèse d’une affection virale ou bactérienne in utero et renvoie pour explication partielle vers le ou les facteurs dits de l’environnement.
Sclérose en plaques: comment vivre avec ?
Il faut veiller aux symptômes et problèmes particulièrement gênants chez le malade présentant une sclérose en plaques : existence d’une infection urinaire latente qui parfois aggrave l’affection, combattre la fatigue et l’asthénie qui sont toujours présentes et liées à l’agent infectieux latent.
le dialogue entre le malade et le médecin ne devra pas éluder un certain nombre de handicaps :
- les problèmes sexuels éventuels ;
- les difficultés motrices pour lesquelles le médecin fera des propositions pragmatiques
- altération de la qualité de vie qui entraîne des tendances dépressives,
- des troubles a minima de la mémoire,
- une asthénie constante liée à l’infection latente.
Il faut permettre au malade d’avoir accès au traitement au bon moment. Aujourd’hui surtout, il faut bien se dire que le diagnostic n’est pas une fatalité, un couperet inexorable. Certaines formes, environ un quart des cas, sont bénignes, et la maladie est actuellement accessible à la médication, même si le traitement complet n’existe pas encore.
Sclérose en plaques: quel traitement ?
Deux traitements sont proposés aux malades, qu’il s’agisse du traitement des poussées ou du traitement de fond :
Le traitement concernant les poussées
Chacun reconnaît le caractère éminemment efficace des perfusions de corticoïdes à fortes doses, en principe en milieu hospitalier. Cette approche thérapeutique présente l’avantage de ne pas exposer aux complications habituelles de la corticothérapie au long cours puisque le traitement est appliqué en séquences courtes.
Le traitement de fond L’interféron bêta 1a et 1b
Il est prescrit soit après la seconde poussée, soit plus tôt si l’on pense que la maladie est évolutive. Le traitement de fond s’appuiera sur l’Interféron bêta (1a ou 1b) qui est un immunomodulateur et non pas immunosuppresseur (qui bloque la réaction immunitaire. Disponible en France depuis 1996, il s’agit du premier traitement efficace dans la prévention des poussées. Il diminue le nombre et la sévérité des rechutes. Il limite donc le handicap fonctionnel, conséquence de chaque poussée. Il est encore trop tôt pour quantifier de façon scientifique le nombre de poussées qui ont pu être évitées par ce traitement de fond mais les auteurs pensent que plus de la moitié d’entre elles sont stoppées ou décapitées. Cet effet bénéfique se traduit à l’IRM (imagerie par résonance magnétique) par une réduction du nombre de nouvelles lésions inflammatoires.
Il semble néanmoins établi que plus de la moitié des patients sous Interféron bêta ne présentent plus aucune poussée et sont donc de parfaits « répondeurs » à ce traitement qu’il importe de poursuivre de façon indéfinie. Le nombre de malades chez qui ce traitement ne semble pas efficace est donc réduit. D’autres médications peuvent alors être proposées en cas d’aggravation.
Ce traitement de fond n’est pas trop astreignant pour le patient. Il existe sous forme soit d’auto-injections sous-cutanées à faire tous les deux jours (interféron bêta 1a, Rebif® ou interféron bêta 1b, Bétaféron®), soit une injection intramusculaire par semaine (interféron bêta 1a uniquement, Avonex®). Au début, les quelques injections initiales peuvent être suivies d’un état pseudo-grippal qui cède après quelques semaines. Un bilan sanguin tous les mois est imposé au départ mais les effets du médicament (effets iatrogènes) portant sur les fonctions sanguines et hépatiques sont rares et transitoires. Par la suite, les consultations de suivi sont plus éloignées dans le temps mais elles doivent se faire à intervalle régulier.
Cette maladie était considérée jusqu’à très récemment comme incurable et particulièrement handicapante. La médecine classique (allopathie) n’ayant aucun traitement adapté à proposer, des pratiques parallèles se sont développées, dont l’intégrité financière et la dimension scientifique sont fortement sujettes à caution. Aujourd’hui, il est d’autant plus recommandé d’éviter ces traitements que nous disposons de médicaments efficaces.
Les thérapeutiques autres que l’interféron
Le copolymère (acétate de glatiramer), sous forme d’injection sous-cutanée quotidienne, diminue d’environ 30 % la fréquence des poussées. Ce produit est un immunomodulateur. Utilisable dans le cadre d’une ATU (autorisation temporaire d’utilisation), donc en milieu hospitalier, ce produit est réservé aux patients présentant une intolérance majeure à l’interféron bêta ou présentant des contre-indications à ce produit (état dépressif sévère, épilepsie mal contrôlée, hypersensibilité aux interférons).
La mitoxantrone a montré son efficacité dans les formes agressives de SEP. Cet immunosuppresseur, prescrit par perfusion intraveineuse mensuelle pendant 6 mois, réduit le nombre de poussées, le niveau de handicap résiduel et le nombre des lésions IRM.
La mitoxantrone apparaît plus comme un recours en cas d’échec de l’interféron bêta. Elle a une toxicité hématologique et cardiaque nécessitant une surveillance de l’hémogramme et une surveillance cardiaque rigoureuse (électrocardiogramme, échographie cardiaque). La dose maximale que l’on peut utiliser sans risque est estimée à 140 mg/m2, soit environ 10 cures de 20 mg par patient. C’est donc un médicament qui ne pourra être utilisé que pendant une période limitée de la vie d’un patient. Ce médicament est disponible dans les hôpitaux, mais il n’a pas encore obtenu en France une autorisation officielle d’utilisation spécifique pour la sclérose en plaques.
Le méthotrexate est un immunosuppresseur déjà utilisé dans d’autres maladies auto-immunes (polyarthrite rhumatoïde) qui peut être proposé dans les formes progressives. Il se présente sous la forme d’une dose unique par semaine par voie orale et nécessite une surveillance rénale et hépatique.
Les immunoglobulines intraveineuses diminueraient la fréquence des poussées dans les formes rémittentes. L’efficacité de ce traitement est encore à l’étude, ne permettant pas de recommander ce traitement en première intention. Ces produits n’ont pas d’AMM dans cette indication. Elles ont un rôle immunomodulateur et il se pourrait qu’à fortes doses, elles favorisent la remyélinisation des lésions du système nerveux central chez l’animal.
L’azathioprine (Imurel®) est un des premiers médicaments immunosuppresseurs utilisés, bien que n’ayant pas d’autorisation de mise sur le marché (AMM) dans le traitement de la SEP. Il aurait une efficacité sur le nombre de poussées dans les formes rémittentes. Son utilisation nécessite une surveillance régulière des fonctions sanguines et hépatiques (prise de sang).
L’antagoniste de l’intégrine alpha-4 est le médicament le plus récent dans le traitement de la SEP (en cours d’évaluation dans les pays anglo-saxons). L’intégrine est une glycoprotéine de surface qui intervient dans l’adhérence des lymphocytes et des monocytes. Ainsi, ces cellules immunitaires ne peuvent plus quitter le réseau sanguin pour s’attaquer au système nerveux du malade. Les premiers résultats semblent encourageants et incitent à poursuivre les essais thérapeutiques.
Sclérose en plaques: nouvelles thérapeutiques
La lésion initiale de la sclérose en plaque est inflammatoire avec une atteinte des graisses de myéline qui entourent les cellules nerveuses : les axanes. Le traitement de base était donc constitué de corticoïdes dont le pouvoir anti-inflammatoire est élevé.
L’évolution de ce processus inflammatoire consiste en la destruction des cellules qui produisent la myéline et qui sont nommées des oligodendrocytes. L’objectif des chercheurs a donc été de chercher les moyens de réduire la destruction de ces cellules.
Deux cytokines ont été identifiées comme ayant ce pouvoir :
- La première se nomme le LIF (facteur inhibiteur de la leucémie). Son action permet de prévenir directement la mort des oligodendrocytes. Les premiers tests chez l’homme semblent corrects et la tolérance à des doses efficaces satisfaisantes ;
- La seconde se nomme le CNTF (facteur neurotrophique ciliaire) et a le pouvoir de potentialiser la survie des oligodendrocytes mais aussi de leur maturation.
Les mécanismes d’action ont été clairement établis. Ces deux découvertes ouvrent la voie à de nouvelles thérapeutiques. Si le trajet avant la mise à disposition reste long et la mesure exacte de l’efficacité reste encore à prouver, c’est un espoir pour les malades atteints de cette maladie pour laquelle la médecine actuelle ne proposerait pas de solutions thérapeutiques pleinement satisfaisantes.